Care este configurația de electroni
configurare atom electronic - distribuția electronilor peste nivelurile de energie și subnivele. Pentru înregistrarea convențională configurația electronică utilizate formule electronice.
Electronic constituie o formulă bazată pe principiul minim de energie și a principiilor Pauli, folosind următorul algoritm:
pentru fiecare punct al numărului de nivelul de energie de electroni utilizând valoarea numerică a numărului cuantic principal n (vezi Tabelul 3.6.);
indica subnivel energie prin litere orbital număr cuantic l (vezi Tabelul 3.6.);
indică numărul total de electroni în subnivelul de energie, cu un număr mic, care este scris în partea din dreapta sus de mai sus caracterul alfabetic cuantic orbital numărul L.
De exemplu, înregistrarea 1s1 - e este o formulă în care un număr mic denotă un electron, care este primul nivel de energie (n = 1), s-subnivel (l = 0). Prin urmare, formula electronică reflectă configurația electronică atom de hidrogen element de H, în care există un singur electron.
configurația electronică 21Sc membru atom scandiu, în care există un electron 21 poate fi scris formula e 1s22s22r63s23r64s23d1 sau într-o altă formă, însumarea tuturor subnivele în nivelurile de energie corespunzătoare:
De electroni formula elementului 21Sc atom se poate observa că învelișul de electroni cuprinde doi electroni s-subnivel al primului nivel de energie (1s2), doi electroni s-subnivel și șase electroni la nivelul a doua energie p-subnivel, adică opt electroni la al doilea nivel ( 2s22r6), doi electroni s-subnivel, șase electroni p-subnivelul, un electron pe nivelul energetic al treilea d subnivel, adică nouă electroni la al treilea nivel energetic (3s23r63d1) și doi electroni s-a patra energie urs subnivel I (4s2).
Uneori, pentru a facilita formulele electronice în loc de simbol atom straturi de electroni intern scrise în paranteze care precede elementul inert. Cel mai apropiat înaintea scandiu 21Sc elementului inert este Argon 18Ar, formula totuși condensat E are forma de scandiu
Pentru un atom poate forma electron-organigrame care arată plasarea electronilor în celule cuantice care indica orbitali. Având în vedere principiul energiei minime este plasat în partea de jos a primului nivel energetic celular orbital (n = 1), deasupra - al doilea (n = 2), apoi - al treilea (n = 3) etc. electroni diagramă flux pentru un atom de 21Sc scandiu descrisă după cum urmează:
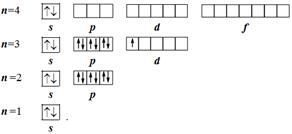
Utilizare și organigrame de electroni reduse, care arată o celulă cuantică straturi electronice numai exterioare. Numărul acestora este determinat de amplasarea formează electroni, adică acel electron care umple ultimul învelișul de electroni al unui atom. Pentru atomul scandiu care formează electroni (№ 21) situat pe 3d-subnivelul, organigrame de electroni, astfel condensat ar trebui să arate două niveluri:
În funcție de ceea ce electroni subnivel energiei care intra formare, elementele sunt împărțite în S, P-, d-, și f-e-familie, îmbinând S, P-, d- și elemente f, respectiv.
Elementele din atomi, care este umplut s-subnivel nivelul de energie exterior, numite s-elemente.
De exemplu, litiu și beriliu sunt s-elemente:
Elementele din atomi, care este umplut cu p-subnivelul a stratului extern, numit elementele p.
De exemplu, elementele carbon și neon sunt elemente p:
Elementele din atomi, care este umplut d-a doua subnivel pe exteriorul nivelului de energie, numit d-elemente.
De exemplu, zece elemente - de la scandiu la zinc - aparțin familiei de d-e și d-elemente sunt, deoarece electronii formând atomii sunt pe d-subnivel:
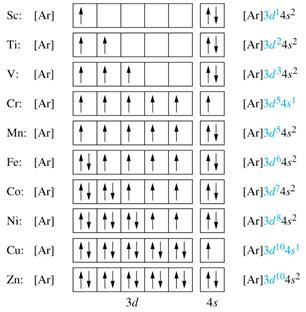
Elementele din atomii de care este umplut cu f-subnivel pe exteriorul celui de al treilea nivel, numite elemente-f.
De exemplu, elementele de ceriu și protactiniu sunt elemente-f:
Exemplul 3.11. Asigurați formula de e-mail și electron - organigrame două nivele de energie din exterior pentru astfel de particule: a) Ar atomi; b) ion S2-; c) ion K +; g) Zn2 + ion. Se specifică particule izoelectronice.
Decizie. Izoelectronice numite particule care au aceeași configurație electronică, astfel încât structura lor este descrisă de aceleași formule și aceleași modele de difracție de electroni electronic.
a) numărul de secvență element de argon (18) indică faptul că atomul Ar are 18 electroni; locație în a treia perioadă - prezența celor trei niveluri de energie, fiind în al optulea grup - numărul de electroni nivel extern egal cu opt, iar subgrupul principal (VIIIA) indică Ar aparținând familiei p-electron. Prin urmare, electroni și electroni formula flowchart pentru cele două straturi exterioare ale elementului atomi de argon are forma
b) Numărul elementului chimic de sulf S este 16, astfel încât atomul S formula electroni
Cu toate acestea, taxa de ioni (-2) arată că în ionul S2- doi electroni înaintea S, adică un atom 16 + 2 = 18. Datorită același număr de atomi de electroni și Ar ion sunt particule S2- izoelectronice și au aceeași formulă și organigramele catodice electronice:
c) Numarul potasiului elementului chimic - 19, deci K atom conține 19 electroni și ioni K + - un electron mai puțin (19-1 = 18). Prin urmare, K + ion este izoelectronice în raport cu atomul de particule și Ar ion S2-, care este evident din formula e K + ion și electron - schema grafică:
g) Ion Zn2 + (№ 30) are doi electroni mai puțin de un atom de zinc, astfel încât cantitatea de ioni Zn2 + de electroni este 30-2 = 28. plasarea lor în învelișul de electroni este descrisă de formula E
și organigrame de electroni două nivele de energie din exterior are forma
De aceea, Zn2 + ion nu este particula izoelectronice atom Ar și ionii de K + și S2-.
Cuvinte cheie și termeni
Care este configurația electronică a atomilor, formula electroni?
Ce elemente se numesc: a) s-elemente; b) elementele p; a) d-elemente;
Sarcini de muncă independentă
Ce formula electronică întâlnește atom Br:
a) 1s22s22r63s23r64s24r5; b) 1s22s22r63s23r64s23d104r5; c) 1s22s22r63s23r64s24r65s24d5; g) 1s22s22r63s23r64s24r65s24d4?
Asigurați-vă formule electronice pentru atomi cu număr atomic de elemente: a) 5; b) 7; c) 9; d) 12; d) 16; e) 21; g) 23; h) 30.
Ultimul electron (formând) astfel elementul atom este descris de numere cuantice: n = 4, l = 1, m = 0, s = + 1/2. Ce este un element: a) Ga; b) Ti; a) Ge; g) Ca?
Ultimul electron (formând) astfel elementul atom este descris de numere cuantice: n = 3, l = 2, m = - 1, s = -1/2. Ceea ce acest element: a) Fe; b) Co; a) Ni; g) Na?
Ultimul electron (formare) în atomul elementului este descris de numerele cuantice:
a) n = 3, l = 1, m = - 1, s = - 1/2; b) n = 2, l = 0, m = 0, s = + 1/2; a) n = 3, l = 2, m = + 2,
s = + 1/2; g) n = 3, l = 0, m = 0, s = + 1/2; d) n = 3, l = 0, m = 0, s = - 1/2.
Asigurați-o formulă electronică a fiecărui element al atomului.